A doksi online olvasásához kérlek jelentkezz be!
A doksi online olvasásához kérlek jelentkezz be!
Nincs még értékelés. Legyél Te az első!
Tartalmi kivonat
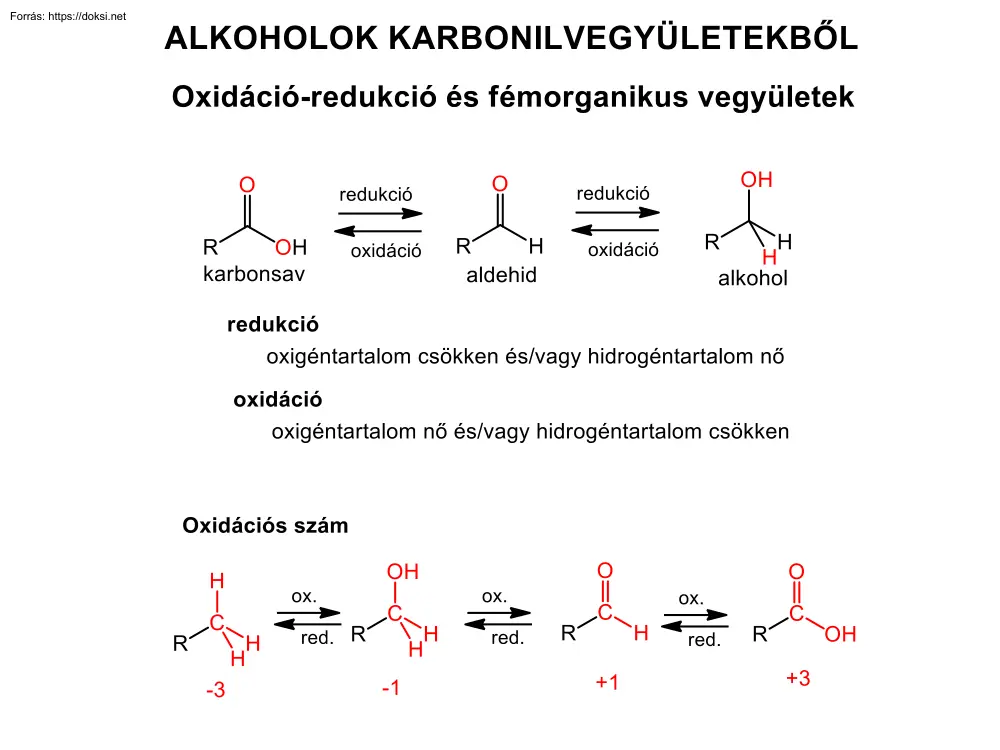
ALKOHOLOK KARBONILVEGYÜLETEKBÖL Oxidáció-redukció és fémorganikus vegyületek 0 R)lOH redukció ► ◄ oxidáció karbonsav 0 R)lH redukció ► ◄ oxidáció aldehid OH R~H H alkohol redukció oxigéntartalom csökken és/vagy hidrogéntartalom nő oxidáció oxigéntartalom nő és/vagy hidrogéntartalom csökken Oxidációs szám H 1 e R/ 'H H -3 OH ox. ◄ ox. 1 e ► red. R/ 'H H -1 ◄ ► red. +1 +3 Redukció litium-aluminium-hidriddel 0 1. LiAIH4 ~ R~OH 2. H2S04 R)lOH primer alkohol karbonsav 0 1. LiAIH 4 • R~OH 2. H2S04 R)lOR' primer alkohol észter OH 0 1. LiAIH4 • R~R' 2. H2S04 R)lR' szekunder alkohol keton Mechanizmus R H '/C=O r1 R' 1- + H-AI-H '----.-/ 1 H R 1. lépés 1 vízmentes közeg (Et2O) 1 H alkoxid ion (2. lépés) -reaktív redukálószer -erős bázis -vízmentes aprotikus oldószer kell - R'-C-0: i H 3o+ R >H-OH R' Redukció
nátrium-borohidriddel 0 R)lH Na8H4 MeOH ► R~OH primer alkohol aldehid 0 OH Na8H4 R)lR' keton MeOH ► R~R' szekunder alkohol Mechanizmus R H R " ~ I /C=O + H-B-H . R'-6-o-: 1 R' ~ 1 H H alkoxid ion H - O H--1►• -kevésbé reaktív, mint a LiAIH 4 -nem szükséges aprotikus oldószer -savak és észterek redukciójára nem alkalmas Reaktivitás R ~CH-OH R' Az alkoholok oxidációja 0 ox. ► primer alkohol 0 ox. 11 11 R~H „ R~OH aldehid karbonsav 0 ox. ► OH R+R" R' tercier alkohol R R' keton szekunder alkohol ox. )l )( ► Krómsavas oxidáció Példa OH aceton ciklooktanon ciklooktanol Mechanizmus 1. addíció 1 „ -C-OH + 1 H 0 11 HO-Cr-OH 11 0 --1►► i 1 --C-0-Cr-OH + H20 1 11 H 0 króm sav-észter 2. elimináció (E2) sebességmeghatározó lépés 1 r'i ) - C - 0 -Cr-OH I J 11 (H H-0 1 H 0 OH E2 1 ► -C=O + + H-0-H 1 H 1 :Cr-OH
11 0 Oxidáció káli u m-permanganáttal H o+ R~OH primer alkohol 3 0 ► 11 R~OH karbonsav Oxidáció piridínium-klorokromáttal CN+-H Cr0 3Cr piridínium-klorokromát PCC 0 R~OH primer alkohol PCC ► R)lH aldehid PCC szekunder alkohol ► keton Fémorganikus vegyületek 1- -C: M 1 ö- + -C: M 1 ö+ 1 - C-M 1 1 ionos (M = Na+, K+) (M = Mg, Li) kovalens (M = Pb, Sn, Hg) Lítiumorganikus vegyületek előállítása R-X + 2 Li Rli + LiX Példa ~Br butil-bromid + 2Li ~Li butil lítium + LiBr Grignard-reagens R-X + Mg Ar- X + Mg reaktivitási sorrend RI > RBr > RCI Példák + Mg /"---sr /"---MgBr etil-magnézium-bromid etil-bromid Br () ~MgBr + Mg V # bróm benzol Szerkezet fenil-magnézium-bromid R. R . 0 1 1 1 1 1 R-Mg-X 1 1 1 1 A Grignard-reagens bázikus jellege 8- ~ R-MgX + H-Y R-H + Mg 2 + + x- + y- A Grignard-reagens nem készíthető az alábbi funkciós csoportok jelenlétében: -OH, NH 2
, -NHR, -COOH, -S0 3 H, -SH, -C==C-H Példák • R-MgX + H-OH ---1► R-H + Mg 2 + + x- + Ho- R-MgX + H-OR ---1► • R-H + Mg 2 + + x- + Ro- R-MgX + HC=CR ---1►► R-H + Mg 2 + + x- + :c=cR A Grignard-reagens reakciója epoxidokkal (oxiránokkal) ►~ R~ ~ ----1 SN2 R-MgX + ~ •• OMgX H o+ 3 ► •• R~ OH primer alkohol Példák V # MgBr + ~ OMgBr H o+ 3 OH ► H o+ 3 kevésbé árnyékolt szénatom ► A Grignard-reagens reakciója karbonilvegyületekkel A OH 0 R-MgBr + 1' 1. éter Mechanizmus (nukleofil addíció) 1. co '-11 ; ;9 2+Br" öö+ ö+ R-MgBr + ~ ~ alkoholát ~ ö- Mg 2+ Br- 2. ~ R alkoholát H + Hs2-H ~ 1' OH alkohol a) Reakció formaldehiddel 0 OH )l H H R-MgBr + H o+ 3 „ -1"1 HR H primer alkohol b) Reakció aldehidekkel 0 R-MgBr + OH ~ H3o+► II R'~H R' R H szek- alkohol c) Reakció ketonokkal R-MgBr +R'~R" -----1►• OH R'J
::~ R ~ HO+ 3 ► R' R" R terc-alkohol d) Reakció észterekkel (2 mol Grignard-reagens jelenlétében) 88+ R-MgBr + (0 '-11 ~+ R' ~ OR" •• + O MgX •• OH - RMgX R' + R R terc-alkohol Példák V MgBr OH + # fenil-magnéziumbromid formaldehid 0 ~ MgBr + etil-magnéziumbromid ,)lH benzil-alkohol OH 1. Et20 2.H 30+ ~ ► acetaldehid bután-2-ol (szek-butil-alkohol) 0 MgBr + ~ butil-magnéziumbromid A aceton OH 1. Et20 2. NH4CI ► 2-metilhexán-2-ol OH 0 2 ~ MgBr etil-magnéziumbromid + ,)lOEI etil-acetát 1. Et20 2. NH4CI ► 3-metilpentán-3-ol Szintézis tervezés Grignard-reakcióval OH ? 3-fenilpentán-3-ol Retroszi ntézis MgBr 0 -> ~ + pentán-3-on (dietil-keton) > ~ fenil-magnéziumbromid MgBr + etil-magnéziumbromid etil-fenilketon OH 0 >2 ~ MgBr + MeO etil-magnéziumbromid metil-benzoát Védőcsoport alkalmazása Retroszintézis HO~ ⇒ H - O ~MgBr ~
nem létképes OH . + Hy o · savas H (védeni kell!) Szintézis HO~Br TBSCI• TBS- O ~ M g B r TBS-0~ ! OH Bu4WF HO~ OH
nátrium-borohidriddel 0 R)lH Na8H4 MeOH ► R~OH primer alkohol aldehid 0 OH Na8H4 R)lR' keton MeOH ► R~R' szekunder alkohol Mechanizmus R H R " ~ I /C=O + H-B-H . R'-6-o-: 1 R' ~ 1 H H alkoxid ion H - O H--1►• -kevésbé reaktív, mint a LiAIH 4 -nem szükséges aprotikus oldószer -savak és észterek redukciójára nem alkalmas Reaktivitás R ~CH-OH R' Az alkoholok oxidációja 0 ox. ► primer alkohol 0 ox. 11 11 R~H „ R~OH aldehid karbonsav 0 ox. ► OH R+R" R' tercier alkohol R R' keton szekunder alkohol ox. )l )( ► Krómsavas oxidáció Példa OH aceton ciklooktanon ciklooktanol Mechanizmus 1. addíció 1 „ -C-OH + 1 H 0 11 HO-Cr-OH 11 0 --1►► i 1 --C-0-Cr-OH + H20 1 11 H 0 króm sav-észter 2. elimináció (E2) sebességmeghatározó lépés 1 r'i ) - C - 0 -Cr-OH I J 11 (H H-0 1 H 0 OH E2 1 ► -C=O + + H-0-H 1 H 1 :Cr-OH
11 0 Oxidáció káli u m-permanganáttal H o+ R~OH primer alkohol 3 0 ► 11 R~OH karbonsav Oxidáció piridínium-klorokromáttal CN+-H Cr0 3Cr piridínium-klorokromát PCC 0 R~OH primer alkohol PCC ► R)lH aldehid PCC szekunder alkohol ► keton Fémorganikus vegyületek 1- -C: M 1 ö- + -C: M 1 ö+ 1 - C-M 1 1 ionos (M = Na+, K+) (M = Mg, Li) kovalens (M = Pb, Sn, Hg) Lítiumorganikus vegyületek előállítása R-X + 2 Li Rli + LiX Példa ~Br butil-bromid + 2Li ~Li butil lítium + LiBr Grignard-reagens R-X + Mg Ar- X + Mg reaktivitási sorrend RI > RBr > RCI Példák + Mg /"---sr /"---MgBr etil-magnézium-bromid etil-bromid Br () ~MgBr + Mg V # bróm benzol Szerkezet fenil-magnézium-bromid R. R . 0 1 1 1 1 1 R-Mg-X 1 1 1 1 A Grignard-reagens bázikus jellege 8- ~ R-MgX + H-Y R-H + Mg 2 + + x- + y- A Grignard-reagens nem készíthető az alábbi funkciós csoportok jelenlétében: -OH, NH 2
, -NHR, -COOH, -S0 3 H, -SH, -C==C-H Példák • R-MgX + H-OH ---1► R-H + Mg 2 + + x- + Ho- R-MgX + H-OR ---1► • R-H + Mg 2 + + x- + Ro- R-MgX + HC=CR ---1►► R-H + Mg 2 + + x- + :c=cR A Grignard-reagens reakciója epoxidokkal (oxiránokkal) ►~ R~ ~ ----1 SN2 R-MgX + ~ •• OMgX H o+ 3 ► •• R~ OH primer alkohol Példák V # MgBr + ~ OMgBr H o+ 3 OH ► H o+ 3 kevésbé árnyékolt szénatom ► A Grignard-reagens reakciója karbonilvegyületekkel A OH 0 R-MgBr + 1' 1. éter Mechanizmus (nukleofil addíció) 1. co '-11 ; ;9 2+Br" öö+ ö+ R-MgBr + ~ ~ alkoholát ~ ö- Mg 2+ Br- 2. ~ R alkoholát H + Hs2-H ~ 1' OH alkohol a) Reakció formaldehiddel 0 OH )l H H R-MgBr + H o+ 3 „ -1"1 HR H primer alkohol b) Reakció aldehidekkel 0 R-MgBr + OH ~ H3o+► II R'~H R' R H szek- alkohol c) Reakció ketonokkal R-MgBr +R'~R" -----1►• OH R'J
::~ R ~ HO+ 3 ► R' R" R terc-alkohol d) Reakció észterekkel (2 mol Grignard-reagens jelenlétében) 88+ R-MgBr + (0 '-11 ~+ R' ~ OR" •• + O MgX •• OH - RMgX R' + R R terc-alkohol Példák V MgBr OH + # fenil-magnéziumbromid formaldehid 0 ~ MgBr + etil-magnéziumbromid ,)lH benzil-alkohol OH 1. Et20 2.H 30+ ~ ► acetaldehid bután-2-ol (szek-butil-alkohol) 0 MgBr + ~ butil-magnéziumbromid A aceton OH 1. Et20 2. NH4CI ► 2-metilhexán-2-ol OH 0 2 ~ MgBr etil-magnéziumbromid + ,)lOEI etil-acetát 1. Et20 2. NH4CI ► 3-metilpentán-3-ol Szintézis tervezés Grignard-reakcióval OH ? 3-fenilpentán-3-ol Retroszi ntézis MgBr 0 -> ~ + pentán-3-on (dietil-keton) > ~ fenil-magnéziumbromid MgBr + etil-magnéziumbromid etil-fenilketon OH 0 >2 ~ MgBr + MeO etil-magnéziumbromid metil-benzoát Védőcsoport alkalmazása Retroszintézis HO~ ⇒ H - O ~MgBr ~
nem létképes OH . + Hy o · savas H (védeni kell!) Szintézis HO~Br TBSCI• TBS- O ~ M g B r TBS-0~ ! OH Bu4WF HO~ OH